الاتحاد الأوروبي يوافق بشروط صارمة على دواء جديد لعلاج الزهايمر
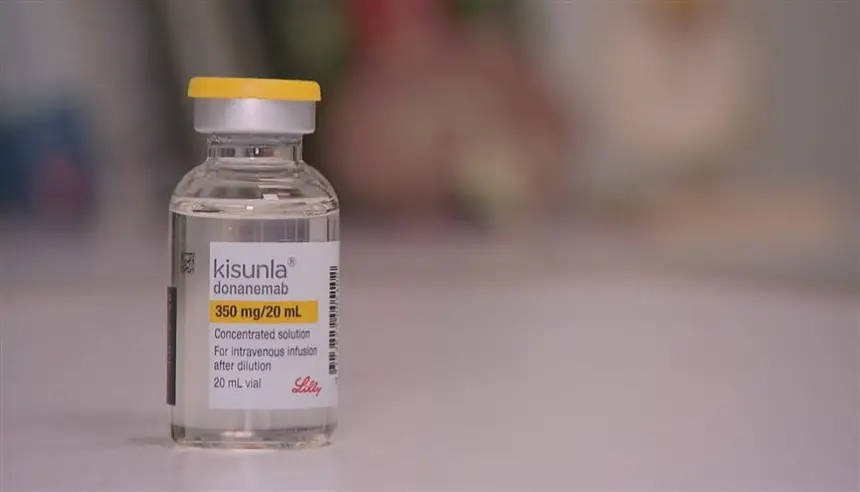
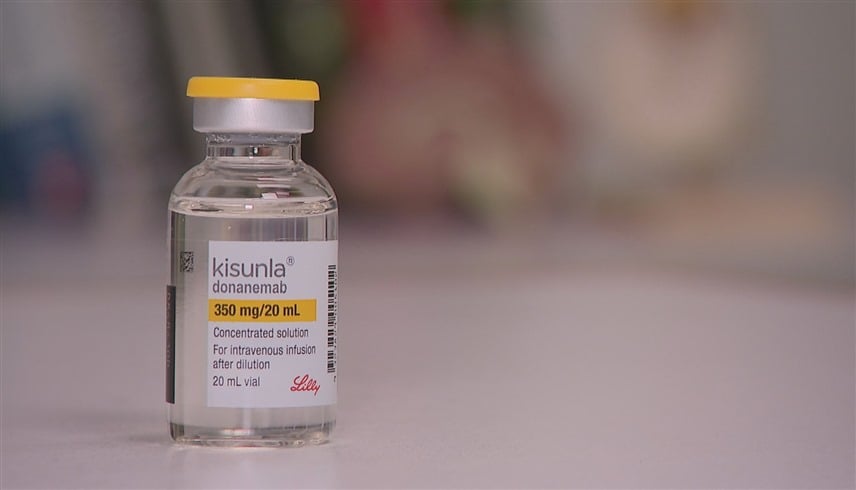
أعلن الاتحاد الأوروبي موافقته المشروطة على دواء "كيسونلا" المخصص لعلاج المراحل المبكرة من مرض الزهايمر، في خطوة أثارت جدلاً واسعاً في الأوساط الطبية. ويأتي القرار مع فرض قيود صارمة، إذ لا يُسمح باستخدام الدواء إلا لدى المرضى الذين لا يحملون طفرات جينية قد تزيد من حدة الآثار الجانبية.
وأكدت المفوضية الأوروبية في بيان رسمي أنها منحت ترخيص تسويق "كيسونلا"، الذي طورته شركة "إيلي ليلي" الأمريكية، لعلاج ضعف الإدراك الخفيف والخرف المبكر المرتبط بالزهايمر. ويحتوي الدواء على المادة الفعالة "دونانيماب"، وهو جسم مضاد حصل في وقت سابق على موافقة في الولايات المتحدة.
ويُعتبر الدواء الجديد أحد أبرز التطورات في مجال علاجات الزهايمر إلى جانب دواء "ليكمبي" من شركتي "بيوجين" و"إيساي"، غير أن الفوائد الفعلية لكلا العلاجين لا تزال موضع نقاش. ففي حين أظهرت التجارب السريرية قدرة على إبطاء التدهور الإدراكي، يرى بعض الخبراء أن هذا التأثير يظل محدوداً ولا يُحدث فارقاً كبيراً في حياة المرضى اليومية.
وتشير تقارير طبية إلى أن هذه الفئة من الأدوية قد تحمل مخاطر جسيمة، مثل النزيف الدماغي والوذمات، ما يجعل الموازنة بين الفوائد والمخاطر أمراً أساسياً قبل وصفها. وتؤكد وكالة الأدوية الأوروبية أن الموافقة المشروطة تهدف إلى ضمان أقصى درجات الحذر مع متابعة نتائج إضافية من الدراسات السريرية.
ويعيد هذا القرار إلى الأذهان مسار دواء "ليكمبي"، الذي حصل على ترخيص تسويق أوروبي نهاية عام 2024 بعد رفض أولي ثم موافقة مشروطة. ويعكس ذلك النهج الحذر الذي يتبناه الاتحاد الأوروبي تجاه العلاجات الجديدة للزهايمر، وسط تزايد الحاجة إلى حلول فعالة لهذا المرض العصبي المتنامي.